Помыткин Артем Николаевич
Клинико-биологические аспекты терапевтического ответа
на ритмическую транскраниальную магнитную стимуляцию
при резистентной шизофрении
3.1.17 -«Психиатрия и наркология»
(медицинские науки)
24.1.188.01
Федеральное государственное бюджетное научное учреждение
«Научный центр психического здоровья»
115522 Москва, Каширское шоссе, 34
Телефон диссертационного совета: (495) 109-03-69
e-mail: dissovet@ncpz.ru
Дата защиты диссертации – 18 декабря 2023 г.
Дата размещения диссертации
на официальном сайте ФГБНУ НЦПЗ – 18 октября 2023 г.
https://ncpz.ru/cond/1/diss/2023/300
На правах рукописи
Помыткин Артем Николаевич
КЛИНИКО-БИОЛОГИЧЕСКИЕ АСПЕКТЫ ТЕРАПЕВТИЧЕСКОГО ОТВЕТА НА РИТМИЧЕСКУЮ ТРАНСКРАНИАЛЬНУЮ МАГНИТНУЮ СТИМУЛЯЦИЮ ПРИ РЕЗИСТЕНТНОЙ ШИЗОФРЕНИИ
3.1.17. — «Психиатрия и наркология»
(медицинские науки)
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва — 2023
Работа выполнена в Федеральном государственном бюджетном научном учреждении «Научный центр психического здоровья».
Научный руководитель:
доктор медицинских наук Каледа Василий Глебович
Научный консультант:
доктор биологических наук Лебедева Ирина Сергеевна
Официальные оппоненты:
Иванов Михаил Владимирович — доктор медицинских наук, профессор, ФГБУ «Национальный медицинский исследовательский центр психиатрии и неврологии им. В.М. Бехтерева» Минздрава России, отделение биологической терапии психически больных, руководитель.
Цукарзи Эдуард Эдуардович — кандидат медицинских наук,
ФГБУ «Национальный медицинский исследовательский центр психиатрии и наркологии имени В.П. Сербского», отделение интенсивной терапии и нелекарственных методов лечения, руководитель.
Ведущая организация: ФГБОУ ВО «Приволжский исследовательский медицинский университет» Минздрава России.
Защита состоится 18 декабря 2023 года в 10:00 на заседании Диссертационного совета 24.1.188.01 в Федеральном государственном бюджетном научном учреждении «Научный центр психического здоровья» по адресу: 115522, Москва, Каширское шоссе, дом 34.
С диссертацией можно ознакомиться в библиотеке и на сайте Федерального государственного бюджетного научного учреждения «Научный центр психического здоровья» http://www.ncpz.ru
Автореферат разослан «___» ноября 2023 г.
Ученый секретарь
диссертационного совета,
кандидат медицинских наук Никифорова Ирина Юрьевна
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы исследования. Изучение резистентности при шизофрении в контексте разработки и совершенствования методов лечения остается актуальным до настоящего времени вследствие высокой распространенности и социальной значимости резистентных состояний. По данным ряда исследователей, распространенность устойчивых к лечению состояний у впервые заболевших пациентов достигает 20-30% [Correll C.U. et al., 2019; Taylor D.M. et al., 2021], а в процессе дальнейшего течения заболевания увеличиваться до 60% [Gillespie A.L. et al., 2017; Kim J.H. et al., 2018].
Внедрение в клиническую практику биологических методов преодоления резистентности, включая клозапин и нейролептики последнего поколения способствовало качественному изменению клинических проявлений шизофрении со снижением частоты встречаемости высокопрогредиентных форм в сторону более благоприятных состояний [Мосолов С. Н. 2012; Тиганов А.С. 2015]. Однако, проблема преодоления резистентности при шизофрении до сих пор остается далекой от разрешения, в пользу чего свидетельствует значительное количество исследований, сосредоточенных на совершенствовании уже существующих противорезистентных мероприятий [Зубов Д.С. 2020; Lally J. et al., 2016; Potkin S.G. et al., 2020], что подчеркивает необходимость развития альтернативных нелекарственных методов.
В качестве одного из основных нелекарственных методов преодоления резистентности традиционно рассматривается электросудорожная терапия, которая имеет ряд ограничений, связанных с декомпенсацией хронических соматических и неврологических заболеваний [Нельсон А.И. 2005], а также высокую вероятность развития стойких когнитивных нарушений [Lisanby S.H. et al., 2000]. При этом наибольшую эффективность ЭСТ показывает в отношении резистентной психотической симптоматики в периоды рецидива заболевания [Baghai T.C. et al., 2008; Lally J. et al., 2019], что ставит вопрос о необходимости поиска более безопасного метода с приоритетным влиянием на инертную симптоматику в периоды стабилизации эндогенного процесса.
В последнее десятилетие ритмическая транскраниальная магнитная стимуляция (рТМС) все чаще рассматривается в качестве метода преодоления резистентности [Маслеников Н.В. и соавт., 2013; Мосолов С.Н. и соавт., 2020, 2023; Aleman A. et al., 2019], который представляет собой неинвазивную стимуляцию головного мозга переменным магнитным полем, позволяющую оказывать модулирующее действие на структуры головного мозга, как в зоне стимуляции, так и за ее пределами посредством функциональных связей между отделами головного мозга.
Степень разработанности темы исследования. Изначально транскраниальная магнитная стимуляция использовалась для лечения депрессивных расстройств, однако высокая клиническая эффективность, наряду с благоприятным профилем побочных эффектов, способствовала интенсивному изучению этого метода при широком спектре психических и неврологических заболеваний. В настоящее время получены доказательства эффективности рТМС в отношении обсессивно-компульсивного расстройства [Rehn S. et al., 2018; Mahmoud A.B. et al., 2022], доказана приоритетность использования рТМС в терапии депрессий в рамках аффективных заболеваниях, при этом эффективности рТМС при депрессиях присвоен уровень доказанности эффекта «А» [Lefaucheur J.P. et al., 2020; Aleman C. et al., 2020].
Исследования рТМС при шизофрении носят более ограниченный характер, а результативность этого метода нуждается в дополнительных исследованиях. Наиболее изученными являются возможности рТМС в отношении вербальных галлюцинаций. Во многих публикациях подтверждена эффективность низкочастотной стимуляции височно-теменной области [Потапов И.В. и др., 2014; Мосолов С.Н. и др., 2023; Li J. et al., 2020], при этом влияние данного метода на другие позитивные симптомы шизофрении, такие как бред, оценивалось крайне редко. Исключение составляет исследование [Saba G., et al., 2006], где изучалось влияние рТМС на бредовые феномены, при этом авторами не было обнаружено достоверных отличий в сравнении с плацебо, что может быть обусловлено использованием низкочастотной стимуляции с подпороговой интенсивностью стимулов, сводящей эффекты магнитного поля к минимуму. Результаты другого исследования [Schreiber S. et al., 2002] свидетельствовали в пользу общего клинического улучшения и уменьшения выраженности позитивных симптомов у пациентов с шизофренией при высокочастотной стимуляции префронтальной коры, однако специальной оценки отдельных позитивных симптомов не проводилось.
Другое важное направление исследований посвящено оценке возможностей рТМС в отношении негативных расстройств и депрессий при шизофрении. К настоящему времени, по данным ряда исследований, [Osoegawa C. et al., 2018; Jiang Y. et al., 2019; Lorentzen R. et al., 2022] получены достоверные данные об эффективности стимуляции префронтальной коры в качестве локуса воздействия в отношении данных расстройств. При этом остаются неразработанными оптимальные параметры стимуляции: часть исследователей склоняется в пользу высокочастотных протоколов, отмечая наряду с основным антинегативным действием также положительное влияние на когнитивное функционирование [Jiang Y. et al., 2019], однако последние исследования отдают предпочтение низкочастотной стимуляции [Lorentzen R. et al., 2022]. В отечественных работах рТМС продемонстрировала отчетливый антинегативный эффект с преимущественным влиянием на эмоциональный компонент негативного синдрома, а также более быстрое развитие тимоаналептического эффекта при тяжелых депрессиях у пациентов с шизофренией по сравнению с лекарственными препаратами, при этом большее влияние рТМС оказывает на вторичную негативную симптоматику и ассоциированную с ней депрессию [Масленников Н.В. и др., 2017].
Таким образом, проведенные исследования рТМС свидетельствуют о безопасности данного метода и благоприятности профиля побочных эффектов у резистентных больных, но данные об эффективности носят противоречивый характер [Wang J. et al., 2013; Aleman A. et al., 2013; Hi S. et al., 2014]. Необходимо отметить, что дизайн проведенных исследований включал в основном низкочастотную рТМС, что с позиций современных взглядов на этот метод полностью не раскрывает его потенциал. Также не проводилось исследований, посвященных влиянию стимуляции на различную симптоматику при резистентной шизофрении, что в свою очередь определят актуальность настоящего исследования.
Цель исследования — выявление комплекса клинико-биологических параметров, определяющих различный терапевтический ответ на ритмическую транскраниальную магнитную стимуляцию при резистентной шизофрении.
Задачи исследования:
- Анализ терапевтической эффективности рТМС при резистентной шизофрении в зависимости от доминирующей психопатологической симптоматики;
- Определение устойчивости терапевтического эффекта при проведении рТМС в зависимости от доминирующей симптоматики;
- Определение профиля безопасности при комбинированном применении рТМС и психотропной терапии;
- Выявление патогенетических факторов, определяющих особенности терапевтического ответа, имеющих прогностическую и терапевтическую значимость.
Научная новизна исследования. До настоящего времени специальных исследований, рассматривающих рТМС, как метод преодоления резистентности при шизофрении, не проводилось. Также в большинстве современных работ внимание сфокусировано на резистентной продуктивной симптоматике в рамках острого периода заболевания [Зубов Д.С., 2020; Мосолов С.Н. и соавт., 2023; Wagner E., et al 2020; Lally J. 2020], в то время как исследований, посвященных преодолению резистентности вне периодов обострения, не проводилось.
Применение рТМС при резистентной шизофрении остается ограниченным, в том числе по причине противоречивости полученных результатов в некоторых крупных исследованиях [Wang J. et. al 2013; Hi S. et al., 2014; Siskind D.J. et al., 2018], а также особенностей дизайна (использование только одного протокола стимуляции), что с позиции современных взглядов на рТМС полностью не раскрывает его потенциал. В настоящем исследовании впервые реализован инновационный селективный подход, а именно выбор методики рТМС на основании клинико-психопатологических особенностей резистентного состояния.
Различия в психопатологической структуре и клинических проявлениях позволило выделить четыре типологических разновидности резистентных состояний: с преобладанием депрессивной симптоматики, с преобладанием галлюцинаторной симптоматики, с преобладанием негативной симптоматики и с преобладанием бредовой симптоматики. Было проведено ранжирование терапевтического эффекта рТМС и выделено три варианта терапевтического реагирования: благоприятная траектория, нейтральная траектория и отрицательная траектория.
Впервые выявлена взаимосвязь между вариантом терапевтического ответа и психопатологической структурой резистентного состояния, а также установлена приоритетность использования метода рТМС с учетом рисков обострения психотической симптоматики.
В рамках мультидисциплинарного исследования был рассмотрен ряд биологических параметров для возможного их использования в качестве предикционных маркеров. По данным нейрофизиологического исследования было обнаружено, что с благоприятной терапевтической траекторией ассоциированы большая когерентность в бета1-поддиапазоне и меньшая исходная спектральная мощность волн тета-диапазона, что совпадает с результатами ряда авторов [Arns M. et al., 2012]. Впервые была проанализирована динамика нейроиммунологического профиля пациентов с резистентной шизофренией и обнаружено соответствие иммунологических показателей выделенным вариантам терапевтического ответа. Установлено, что наиболее эффективным курс рТМС оказался у пациентов с умеренным повышением активности ЛЭ и α1-ПИ и отсутствием аутоиммунного компонента. Напротив, изначально высокий уровень воспалительных и аутоиммунных реакций, сопряжен с низкой эффективностью рТМС и сопровождается отрицательной динамикой иммунологических показателей. Нейропсихологическое исследование позволило выявить три типа нейропсихологических симптомокомплексов, соответствующих трем терапевтическим траекториям: для благоприятной траектории характерен комплекс нарушений избирательности психических процессов, связанный с дисфункцией правого полушария; для нейтральной – нарушения регуляции произвольной деятельности, обработки слухоречевой информации, а также нарушения пространственного анализа и синтеза; для отрицательной – комплекс выраженных нарушений произвольной регуляции мыслительных процессов, связанный с дисфункцией префронтальной коры левого полушария.
Теоретическая и практическая значимость исследования. В проведенном исследовании нашла решение актуальная для психиатрии задача – повышение качества терапевтического ответа при резистентной шизофрении. Результаты работы свидетельствуют о том, что рТМС может рассматриваться в качестве показания для лечения резистентных состояний при шизофрении. Продемонстрирована высокая клиническая эффективность метода при лечении депрессивных и галлюцинаторных расстройств, умеренно выраженное положительное влияние на негативную симптоматику. Установлена ограниченная возможность использования рТМС для преодоления резистентности в отношении бредовой симптоматики. Практическую значимость имеют данные о динамике разрешения различных по структуре состояний, а также данные о стабильности достигнутых результатов при резистентных состояниях с доминированием депрессивной и галлюцинаторной симптоматики, неустойчивости эффекта при состояниях с доминированием негативной симптоматики. Учитывая профиль нежелательных явлений и риск их развития, была определена тактика ведения пациентов после курса рТМС. Изучение нейроиммунологического, нейрофизиологического и нейропсихологического профилей пациентов с резистентной шизофренией способствовало выявлению наиболее информативных параметров предикции эффектов терапии, что может быть успешно внедрено в клиническую практику.
Методологические принципы, лежащие в основе проведенного исследования, могут быть использованы как в научной, так и в практической деятельности врачей-психиатров. Результаты диссертационного исследования имеют практическую значимость для совершенствования терапии пациентов с резистентной шизофренией.
Методология и методы исследования. Теоретической и методологической основой являлись отечественные и зарубежные исследования, посвященные изучению резистентной шизофрении и методам преодоления терапевтической резистентности [Малин Д.И. 2003; Мосолов С.Н. 2012; 2023; Faden J. et al., 2018; Correll C.U. et al., 2021]. Настоящее исследование выполнено в отделе юношеской психиатрии (рук. — д.м.н., В.Г. Каледа) и лаборатории нейровизуализации и мультимодального анализа (рук. — д.б.н. И.С.Лебедева) ФГБНУ НЦПЗ (директор — проф., д.м.н. Т.П. Клюшник) в период с 2015 по 2022 гг. Общую выборку составили 88 пациентов мужского пола, которые проходили стационарное лечение в связи с наличием резистентных психопатологических расстройств в структуре шизофрении.
Критерии включения: диагноз шизофрении по МКБ–10 (F20.0, F20.4, F20.5); резистентность психопатологической симптоматики; манифестация заболевания с психотическими проявлениями в юношеском возрасте; наличие добровольного информированного согласия.
Критерии невключения: наличие выраженной психотической симптоматики на момент включения в исследование; сопутствующие психические, соматические и неврологические заболевания, затрудняющие проведение исследования; обострение инфекционно-воспалительных и аутоиммунных заболеваний в течение 2-х месяцев до включения в исследование.
Использовались следующие методы: клинико-психопатологический (оценка проводилась ежедневно на всем протяжении исследования, 0-42 день); психометрический (0, 21 и 42 день), использовались шкалы: PANSS, SANS, CDSS, AHRS, CGI-S, CGI-I; нейрофизиологический[1] (анализ исходной фоновой ЭЭГ и вызванных потенциалов, 0 день); нейропсихологический[2] (0 день); нейроиммунологический[3] (технология «Нейроиммунотест», 0 и 21 день); статистический.
Исследование проведено в соответствии с Хельсинской декларацией по вопросам медицинской этики с соблюдением прав, интересов и личного достоинства участников. Проведение исследования одобрено Локальным этическим комитетом ФГБНУ НЦПЗ (протокол № 251 от 15.12.2015).
С учетом современных подходов к установлению резистентности при шизофрении были использованы следующие критерии: отсутствие отчетливой положительной динамики после двух последовательных курсов антипсихотической терапии препаратами разных фармакологических групп (в течение 6-8 недель) в дозах от среднетерапевтических до максимально допустимых, с учетом индивидуальной переносимости, а также при условии контроля за приёмом препаратов [Мосолов С.Н. 2012; Howes O.D. et al., 2017; Faden J., Citrome L., 2019].
На первом этапе исследования (0 день) происходил отбор пациентов с шизофренией, соответствующих критериям резистентности. С позиций ведущей психопатологической симптоматики было выделено четыре типологические разновидности: 1 разновидность – с преобладанием депрессивной симптоматики (n=22), 2 разновидность – с преобладанием галлюцинаторной симптоматики (n=24), 3 разновидность – с преобладанием негативной симптоматики (n=22), 4 разновидность – с преобладанием бредовой симптоматики (n=20). Пациенты были рандомизированы в две группы – основная и контрольная, включавшие в себя равное количество наблюдений из всех разновидностей резистентных состояний. Пациенты основной группы (44 человека) получали комбинированное лечение, состоящее из курса рТМС и психофармакотерапии, в контрольной группе (44 человека) пациенты получали только психотропную терапию. В обеих группах пациенты продолжали получать терапию, подобранную до начала исследования, коррекции лечения не проводилось для исключения влияния данного фактора на оценку эффективности рТМС. Отсутствие коррекции лечения в период проведения стимуляции было допустимо в связи со стабильностью психического состояния данной когорты больных.
На втором этапе исследования (1-21 день) больные основной группы получали 15 сеансов рТМС. Для каждой типологической разновидности использовался отдельный протокол рТМС, выбор которого осуществлялся на основании литературных данных и учитывал наряду с наибольшей гипотетической эффективностью в отношении конкретных психопатологических образований, также безопасность данных параметров для пациентов. В связи с отсутствием в литературе методик стимуляции для резистентной симптоматики, в исследовании использовались протоколы эффективные в отношении психопатологических образований не имеющих признаков резистентности. При 1 и 3 разновидности проводилась высокочастотная стимуляция левой дорсолатеральной префронтальной коры (лДЛПК) [Zhao S. et al., 2014; Kang J. et al., 2016], при 2 разновидности использовался протокол низкочастотной стимуляции височно-теменной области [Bais L. et al., 2014], при 4 разновидности был выбран протокол высокочастотной стимуляции лДЛПК, в связи с ограниченностью исследований влияния рТМС на бредовую симптоматику, а также единичным положительным опытом высокочастотной стимуляции [Wobrock T. et al., 2015].
Критерием, свидетельствующем о терапевтической эффективности рТМС, было снижение общей выраженности симптоматики по шкале PANSS на 20% и более, в соответствии с клиническими рекомендациями Российского общества психиатров «Шизофрения F20» (2019).
На третьем этапе исследования (22-42 день) проводилась оценка стойкости терапевтического эффекта.
Основные положения, выносимые на защиту:
- Ритмическая транскраниальная магнитная стимуляция является эффективным методом преодоления терапевтической резистентности при шизофрении. Совместное применение рТМС с психофармакотерапией приводит к более выраженной редукции симптоматики по сравнению с лечением психотропными препаратами.
- Ритмическая ТМС является безопасным методом немедикаментозной терапии, а большинство нежелательных явлений не требует изменения тактики лечения.
- Для прогнозирования результатов лечения необходим комплексный клинико-биологический подход, включающий клинико-психопатологическую оценку, анализ исходной фоновой ЭЭГ и вызванных потенциалов, определение воспалительных и аутоиммунных маркеров, а также исследование особенностей нейрокогнитивного функционирования.
Степень достоверности и апробация результатов исследования.
Достоверность научных положений и выводов достигнута благодаря репрезентативности данных, а также комплексной методике обследования, включающей клинико-психопатологический, психометрический, клинико-иммунологический, нейрофизиологический, нейропсихологический и статистический методы. Результаты проведенного исследования полностью соответствуют специальности «Психиатрия и наркология» — 3.1.17.
Основные положения диссертации представлены на Всероссийской конференции с международным участием, посвященной 75-летию Научного центра психического здоровья (7 июня 2019 г., Москва); на European Congress of Psychiatry (10-13 апреля 2021 год, Флоренция, Италия); на XVII Съезде психиатров России «Интердисциплинарный подход к коморбидности психических расстройств на пути к интегративному лечению» (15-18 мая 2021 год, Санкт-Петербург); на Всероссийской школе молодых психиатров «Суздаль-2021» (23–27 сентября 2021, Суздаль); на конференции, посвященной памяти академика А.В. Снежневского (25 мая 2022, Москва); на 5-ой Костромской Всероссийской школе молодых ученых в области психического здоровья (6–8 октября 2022, Кострома), на Всероссийской Школе молодых психиатров "Суздаль-2023" (13-17 апреля 2023 год, Суздаль).
Личный вклад автора. Автором лично были выполнены все этапы исследования: разработан его дизайн, определены цель и задачи, проведен анализ актуальной научной литературы, проведен сбор материала и обработка данных и их статистический анализ. Автором были сформулированы выводы и практические рекомендации, подготовлены к публикации результаты по теме исследования. Полученные результаты были оформлены автором в виде диссертационной работы.
Апробация диссертации состоялась 04 июля 2023 года на межотделенческой конференции ФГБНУ НЦПЗ.
Внедрение результатов исследования. Результаты данного исследования нашли применение в практической работе клиники ФГБНУ НЦПЗ, а также филиалов ГБУЗ «ПКБ № 4 ДЗМ» «ПНД №8», «ПНД №9».
Публикации результатов исследования. Основные результаты исследования изложены в 9 публикациях, 7 работ размещены в рецензируемых изданиях, рекомендованных ВАК для диссертационных материалов, в том числе 5 статей в журналах, индексируемых в Scopus.
Объем и структура диссертации. Диссертация изложена на 252 страницах машинописного текста (основной текст составляет 167 страниц, приложение – 85 страниц), работа состоит из введения, 4 глав, заключения, выводов, списка литературы, практических рекомендаций и клинических наблюдений. Приведено 20 таблиц, 33 рисунка и 4 клинических наблюдения. Библиографический указатель содержит 291 источник (из них 62 отечественных, 229 иностранных).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
В результате проведенного исследования было установлено, что комбинированную терапию (рТМС и психофармакотерапию) следует рассматривать как эффективный и безопасный метод преодоления резистентности при шизофрении, при этом динамика ряда биологических параметров имеет важное прогностическое значение и соответствует различному по выраженности эффекту лечения.
Было выделено три варианта терапевтической траектории: благоприятная (отчетливая положительная клиническая динамика и редукция симптоматики по PANSSS более 20%), нейтральная (отсутствие существенной клинической динамики, редукция симптоматики по PANSS менее 20% или повышение оценок психометрических шкал менее чем на 10%), отрицательная траектория (клинически значимое ухудшение состояния, утяжеление симптоматики по PANSS более 10%).
Было выявлено, что к благоприятной траектории на момент окончания курса рТМС (21 день) относились 34,1% пациентов (n=15), при этом к завершению исследования (42 день) – 40.9% (n=18). Нейтральной траектории после окончания стимуляции соответствовало 40,9% пациентов (n=18), а к окончанию исследования 52,3% (n=23). К отрицательной траектории к 21 дню исследования было отнесено 25,0% (n=11), а к 42 дню 6,8% (n=3). Распределение исходов лечения по терапевтическим траекториям к 42 дню в большей степени отражало потенциал рТМС – стойкость эффекта, а также его отсроченность в зависимости от клинико-психопатологических особенностей текущего состояния.
При разновидности резистентного состоянияс преобладанием депрессивной симптоматики (n=11) к 21 дню 54,6% пациентов были отнесены к благоприятной траектории, 45,5% к нейтральной траектории. К окончанию исследования (42 день) наблюдалось увеличение количества положительных исходов: 63,6% пациентов соответствовали благоприятной траектории и 36,4% нейтральной траектории. Наблюдавшееся повышение количества благоприятных исходов (р<0.05), свидетельствует об отсроченности терапевтического эффекта при разрешении депрессивных состояний, характерного в целом для применения рТМС у пациентов с шизофренией [Shi C. et al., 2014; Li Z. et al., 2016]. У пациентов данной разновидности в структуре депрессии, наряду с устойчивой гипотимией, основное место занимали явления негативной аффективности [Смулевич А.Б. и соавт., 1997; 2004].
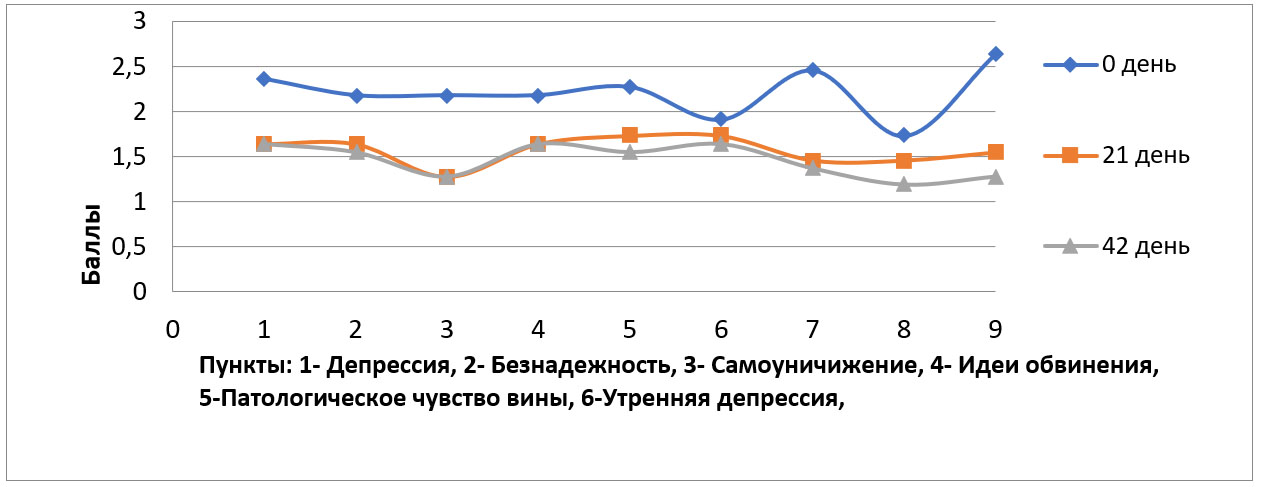
Рисунок 1. Динамика состояния по шкале CDSS в основной группе за весь период исследования при 1 разновидности
Динамика разрешения депрессивного состояния обнаруживала некоторое опережающее влияние на двигательную сферу по сравнению с тимическим компонентом. Качественное улучшение определялось как на клиническом уровне, так и по данным психометрии.
Пациенты основной группы к окончанию исследования демонстрировали статистически достоверную редукцию по общему баллу PANSS в диапазоне 16,7%-38,9% (ср. значение 26,1% p=0.002), выраженность депрессивной симптоматики по шкале CDSS (рисунок 1) уменьшилась на 27,8-52,4% (ср. значение 34,7%; p=0.006), в то время как состояние пациентов контрольной группы оставалось без значимой динамики (p>0,05). Спектр побочных эффектов в основном ограничивался алгическими ощущениями, за исключением инверсии аффекта в одном наблюдении.
В отличие от других работ, где влияние рТМС на депрессивную симптоматику имело «транзиторный» характер [Geller V., et al., 1997], либо обнаруживалась высокая истощаемость эффекта [Масленников Н.В. и соавт., 2017; Mosolov S.N. et al., 2017], в проведенном исследовании был получен выраженный и стойкий терапевтический эффект.
При разновидности спреобладаниемгаллюцинаторной симптоматики (n=12) к 21 дню исследования отмечалось равное соотношение случаев благоприятной и нейтральной траектории (41,7%), при этом к отрицательной траектории были отнесены 16,7% исходов лечения. К 42 дню исследования отмечалось увеличение до 50% случаев, соответствовавших благоприятной траектории, сокращение представленности отрицательной траектории до 8,3% и сохранение значений нейтральной траектории (41,7%). К отрицательной траектории пациенты были отнесены в связи с развитием в одном из наблюдений субъективно значимых нежелательных явлений (болезненные ощущения в месте стимуляции), нивелирующие положительные эффекты лечения, а также в связи с актуализацией психотической симптоматики в одном случае.
На момент включения в исследование галлюцинаторные расстройства доминировали в клинической картине и характеризовались непрерывностью, стереотипностью и обыденностью содержания. В результате проведенного курса лечения было выявлено относительно изолированное влияние рТМС на вербальные галлюцинации. Отмечалось постепенное развитие эффекта, начальные проявления которого относились ко второй половине курса, при этом после завершения рТМС достигнутый эффект сохранился в полном объеме. Наиболее заметное влияние стимуляция оказала на объем галлюцинаторной продукции: сокращалась продолжительность эпизодов галлюциноза, а также количество галлюцинаций в течение дня, что снизило отчетливое дезадаптирующее влияние данной симптоматики на пациентов. Помимо основного эффекта отмечалось умеренное седируюшее и анксиолитическое действие, что находило отражение в уменьшении загруженности переживаниями и уменьшении напряженности.
Редукция симптоматики к 42 дню исследования по общей оценке PANSS была в диапазоне 12,1-22,5% (в среднем 19,3%; р=0,005), а по общему баллу профильной шкалы AHRS (рисунок 2) находилась в диапазоне 9,5-45,8% (ср. значение 20,1%; p=0,002). Полученные результаты комбинированного применения психофармакотерапии и рТМС продемонстрировали преимущество над психофармакотерапией в контрольной группе, где не отмечалось отчетливой динамики. При этом имелись достоверные межгрупповые различия, так, в среднем, значения общего балла по PANSS в основной группе были на 11,4% ниже к 21 дню, (p=0,03) и на 11,3% к 42 дню (p=0,02), по шкале AHRS ниже на 26,2% (p=0,002) после стимуляции и на 20,5% (p=0,003) в конце исследования.
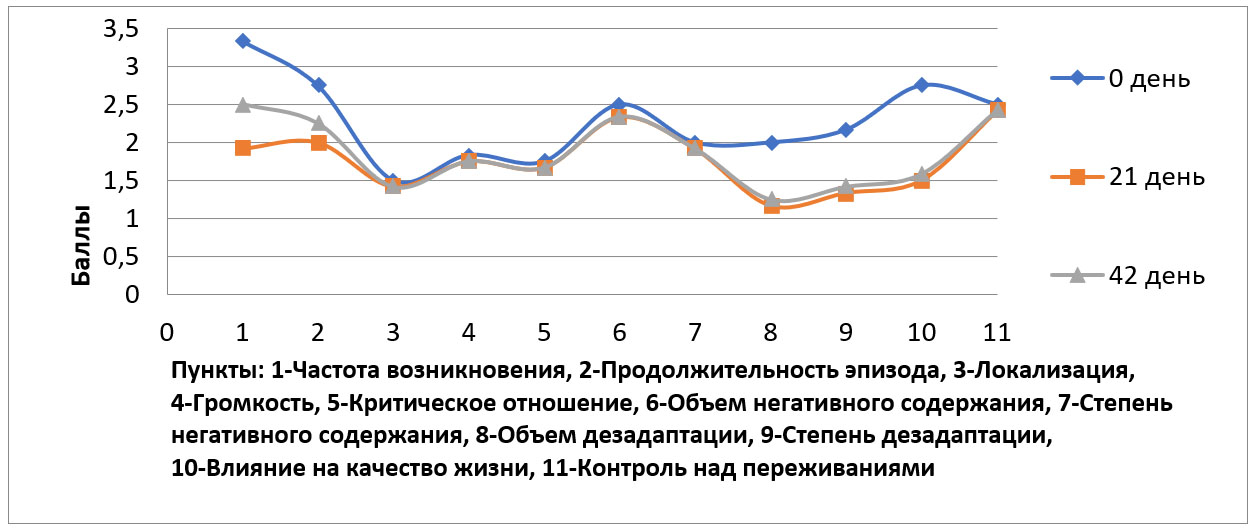
Рисунок 2. Динамика состояния по шкале в основной группе за весь период исследования при 2 разновидности
Результаты исследований других авторов со схожим дизайном имеют сопоставимые с данной работой результаты по количеству пациентов, ответивших на лечение (31,6%-52%) [Dollfus S. et al., 2020; Potapov I.V. et al., 2022], однако в большинстве работ не оценивалась продолжительность терапевтического эффекта, за исключением серии исследований R.E. Hoffman et al., (2003; 2013; 2015), результаты которых свидетельствуют о стабильности эффектов низкочастотной стимуляции височно-теменной области, что также получило подтверждение в данном исследовании.
При разновидности с преобладанием негативной симптоматики (n=11) к 21 дню исследования 36,4% случаев соответствовали благоприятной траектории (к 42 дню – 18,2%), 54,6% – нейтральной траектории (к 42 дню – 81,8%), 9,1% – отрицательной траектории (к 42 дню – 18,2%). Полученные результаты отражают постепенную утрату терапевтического эффекта, связанную с прекращением стимуляции, что, судя по данным некоторых публикаций, свидетельствует о недостаточном по продолжительности курсе стимуляции [Mogg A. et al., 2007; Quan W.X. et al., 2015] в отношении негативной симптоматики.
Изначально при данной разновидности резистентных состояний негативная симптоматика носила персистирующий характер и была представлена преимущественно нарушениями эмоционально-волевого спектра. Влияние рТМС на клинические проявления негативных расстройств было наиболее заметным в сфере мотивации.
Описанные в настоящем исследовании особенности влияния на негативную симптоматику обнаруживали транзиторный характер. Достоверные отличия были получены только к моменту окончания стимуляции (21 день). Снижение общей оценки по шкале PANSS в основной группе находилось в диапазоне 7,7%-18,3% (12,5%, p=0.01). При рассмотрении динамики по профильной шкале SANS (рисунок 3) обнаруживалось приоритетное влияние рТМС на симптомы «аффективное уплощение» со снижением выраженности симптоматики на 25,3% (p=0,001), «алогии» на 15,0% (p=0,002), «абулии-апатии» на 37,0% (p=0,001). При этом ослабление негативных расстройств, соответствовавшее редукции 19,5% общей оценки по SANS (p=0,007), было ниже, чем в среднем по данным исследований со схожим дизайном (25-34%) [Suhua Z. et al., 2014; Zhuo K. et al., 2019].
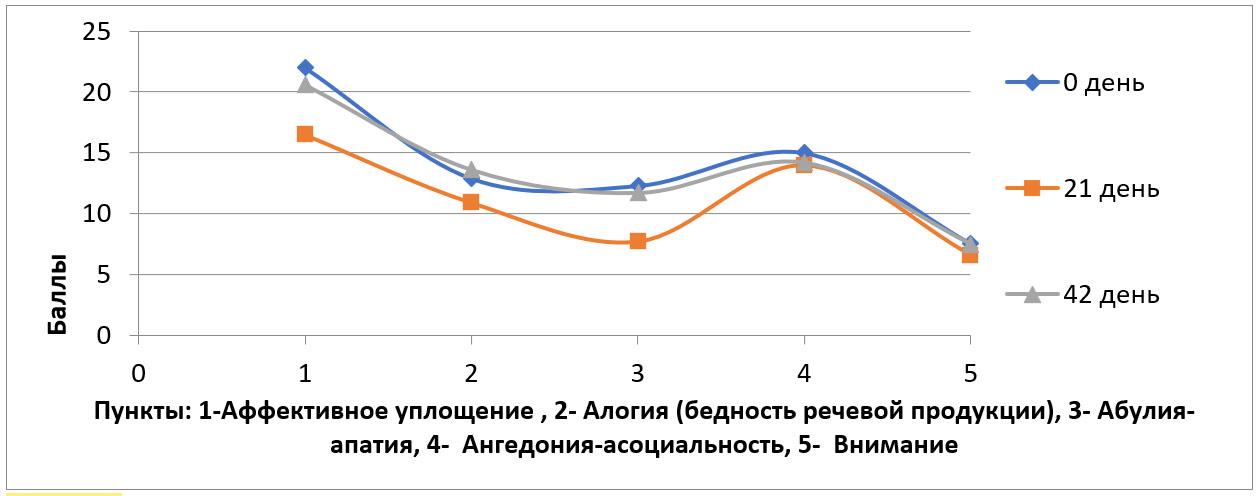
Рисунок 3. Динамика состояния по шкале в основной группе за весь период исследования при 3 разновидности
Отличия основной и контрольной группы имели статистическую достоверность только к 21 дню исследования (p<0,05).
При разновидности с преобладанием бредовой симптоматики (n=10) распределение пациентов по терапевтическим траекториям к 21 дню исследования демонстрировало ухудшение состояния на фоне проведения курса рТМС – 80,0% пациентов соответствовали отрицательной траектории, 20,0% – нейтральной. К 42 дню исследования, после проведения купирующей терапии, 30,0% пациентов были отнесены к положительной траектории в связи с развитием улучшения на фоне лечения. В 50,0% наблюдений исход лечения соответствовал нейтральной траектории, в 20,0% - отрицательной.
На момент включения пациентов в исследование психический статус исчерпывался стабильной картиной хронических бредовых расстройств с персекуторными идеями, сопровождающимися бредовым аффектом, негативизмом и замкнутостью. Окончание стимуляции в основной группе соответствовало повышению общего балла PANSS на 9,7% (p=0,007), а также увеличению оценок в кластерах возбуждения на 24,0% (p=0,002) и параноидных расстройств на 40,6% (p=0,002). Однако к моменту завершения исследования (42 день) общая оценка по PANSS снизилась на 5,43% (p=0,01), шкале позитивных синдромов на 15,4% (p=0,002), кластеру параноидных расстройств на 17,0% (p=0,038) и кластеру возбуждения на 11,3% (p=0,016), по сравнению с началом исследования, что свидетельствовало об эффективности психотропной терапии и преодолении резистентности (рисунок 4). В основной группе, в сравнении с контрольной, на 21 день исследования было обнаружено статистически значимое (p<0,05) повышение баллов на 16,9% в «кластере возбуждение», на 27,7% в «параноидном кластере» и на 18,5% по шкале позитивных синдромов. Однако к окончанию исследования все выбранные для анализа параметры в основной группе были достоверно ниже (p<0,05).
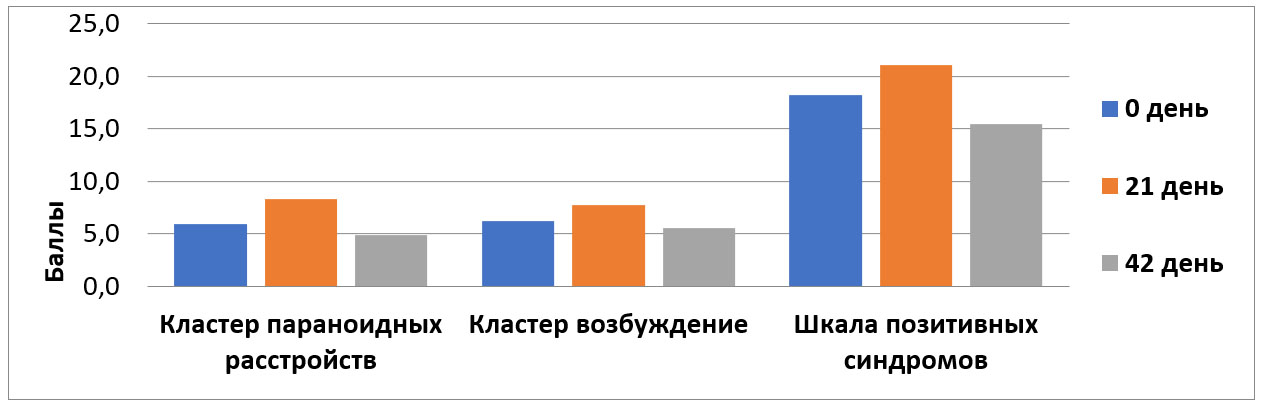
Рисунок 4. Динамика состояния по шкале PANSS в основной группе при 4 разновидности
Для объективизации клинических эффектов рТМС, а также получения представления о биологических параметрах, имеющих предиктивную значимость, в рамках мультидисциплинарного подхода было проведено исследование иммунологических, нейрофизиологических и нейропсихологических показателей.
Результаты нейрофизиологического исследования выявили несколько потенциально значимых показателей, ассоциированных с клиническим эффектом. К ним относились исходно большая когерентность в бета1-поддиапазоне и меньшая спектральная мощность тета-диапазона. Большая когерентность в бета1-поддиапазоне отражает менее выраженные нарушения в работе нейронных сетей [Higashima M. et al., 2007] ассоциировалась в настоящем исследовании с более выраженной редукцией психопатологической симптоматики. Тета-активность связывают с процессами взаимодействия между гиппокампом и префронтальной корой [Colgin L.L. 2011; Benchenane K. et al., 2011] и, таким образом, большее нарушение соответствующих функциональных и структурных нейронных сетей может быть прогностически неблагоприятным явлением.
Результаты нейроиммунологическогоисследования свидетельствуют, что для благоприятной терапевтической траектории было характерно исходное незначительное повышение активности ЛЭ и α1-ПИ по сравнению с нормой (p<0,05), в дальнейшем отмечалась относительная нормализация иммунологических показателей, что является объективным маркером снижения интенсивности патологического процесса в мозге [Клюшник Т.П. и соавт., 2020]. При отрицательной траектории изначально обнаруживалась низкая активность ЛЭ и наличие аутоиммунного компонента к ОБМ, при этом для нейтральной траектории было характерным выраженное повышение активности ЛЭ и α1-ПИ по сравнению с нормой (p<0,05).
Нейропсихологическое исследование позволило выделить три типа нейропсихологических симптомокомплексов, соответствующих трем терапевтическим траекториям: для благоприятной траектории был характерен комплекс нарушений избирательности психических процессов, связанный с дисфункцией правого полушария; для нейтральной – нарушение регуляции произвольной деятельности, обработки слухоречевой информации, а также нарушения пространственного анализа и синтеза разной степени выраженности; для отрицательной – комплекс выраженных нарушений произвольной регуляции мыслительных процессов, связанный с дисфункцией префронтальной коры левого полушария.
Таким образом, при определении тактики и объема медицинской помощи больным с резистентной шизофренией, в соответствии с полученными в настоящей работе результатами клинических и параклинических исследований, комбинированное лечение (рТМС и психофармакотерапию) следует рассматривать как эффективный метод преодоления резистентности, особенно у тех пациентов, где проведение других противорезистентных мероприятий ограничено в связи с риском декомпенсации хронических заболеваний или сопряжено с опасными побочными эффектами.
ЗАКЛЮЧЕНИЕ
Результаты проведенного исследования клинико-биологических аспектов терапевтических эффектов рТМС при резистентной шизофрении позволяют сформулировать следующие выводы:
- Ритмическую транскраниальную магнитную стимуляцию (рТМС) в сочетании с психофармакотерапией необходимо рассматривать как эффективный метод преодоления резистентности при шизофрении. В 34,1% наблюдений к концу курса стимуляции (21 день) применение комбинированной терапии характеризовалось благоприятной терапевтической траекторией – приводило к преодолению резистентности и отчетливой редукции психопатологической симптоматики (p<0,05). При этом нейтральная терапевтическая траектория (без значимой динамики состояния) наблюдалась в 40,9% случаев, а отрицательная терапевтическая траектория (с ухудшением состояния) отмечалась в 25,0% случаев. Эффективность рТМС зависела от доминирующей психопатологической симптоматики, что позволило выделить четыре разновидности резистентного состояния: с преобладанием депрессивной симптоматики (1 разновидность), с преобладанием галлюцинаторной симптоматики (2 разновидность), с преобладанием негативной симптоматики (3 разновидность), с преобладанием бредовой симптоматики (4 разновидность).
1.1 На фоне проведения рТМС наиболее выраженная положительная динамика была характерна для 1 разновидности, в 54,6% наблюдений отмечалась благоприятная терапевтическая траектория, в 45,5% случаев – нейтральная терапевтическая траектория; редукция симптоматики по шкале PANSS составила 25.2% (p<0,05), а выраженность депрессивной симптоматики по шкале CDSS снизилась на 29,6% (p<0,05).
1.2. При 2 разновидности отмечался менее выраженный положительный эффект, количество наблюдений, соответствовавших благоприятной терапевтической траектории, составило 41,7%, нейтральной терапевтической траектории – 41,7%, в 16,7% случаев наблюдалась отрицательная траектория; общая оценка по шкале PANSS снизилась на 12,5% (p<0,05), а по профильной шкале AHRS на 22,5% (p<0,05).
1.3. При 3 разновидности в 36,4% случаев наблюдалась благоприятная траектория, 54,6% – нейтральная траектория, в 9,1% – отрицательная траектория; снижение общей оценки по шкале PANSS составило 12,5%, (p<0.05), по профильной шкале SANS 19,5% (p<0.05);
1.4. При 4 разновидности наблюдалось утяжеление психотической симптоматики к 21 дню исследования: 80,0% наблюдений соответствовали отрицательной траектории, 20,0% – нейтральной; повышение общей оценки PANSS составило 9,7% (p<0.05).
- К концу посткурсового наблюдения (42 день) отмечалось увеличение случаев благоприятной терапевтической траектории до 40,9%, нейтральной терапевтической траектория до 52,3% и уменьшение отрицательной терапевтической траектории до 6,8% случаев. Устойчивость терапевтического эффекта рТМС напрямую зависела от клинико-психопатологических особенностей резистентного состояния.
2.1. Наиболее стабильный результат лечения был достигнут при 1 разновидности, где отсутствовали случаи отрицательной терапевтической траектории, при этом в период посткурсового наблюдения (22-42 день) сохранялась положительная тенденция, с увеличением благоприятной терапевтической траектории до 63,6% (на 9,0%).
2.2. При 2 разновидности отмечался стабильный терапевтический эффект, при этом в периоде посткурсового наблюдения (22-42 день) отмечалось повышение исходов лечения благоприятной терапевтической траектории до 50,0% (на 8,3%).
2.3. При 3 разновидности отмечался нестабильный положительный эффект, что подтверждалось сокращением исходов лечения, соответствовавших благоприятной терапевтической траектории до 18,2% за период посткурсового наблюдения (22-42 день), при этом при данной разновидности отсутствовали случаи с отрицательной терапевтической траекторией.
2.4. При 4 разновидности резистентного состояния отмечались отчетливые положительные тенденции, характеризовавшийся появлением случаев положительной траектории в 30% наблюдений, сокращением до 20,0% (на 60,0%) представленности отрицательной траектории, увеличением до 50,0% (на 30,0%) исходов в рамках нейтральной траектории, что отражало как индивидуальные особенности вариабельности эффекта, так и его лабильность в рамках данной типологической разновидности.
- Нежелательные явления, обусловленные влиянием магнитного поля на ткани головы (боль или дискомфорт в месте стимуляции), отмечались в 41,0% случаев, но имели благоприятное течение, не требовавшее прекращения стимуляции, при этом их максимальная выраженность приходилась на начало курса лечения с последующей постепенной редукцией нежелательных явлений. Развившееся у ряда пациентов (20,4%) субпсихотическое состояние, несмотря на его благоприятное течение, свидетельствовало о необходимости особой осторожности проведения рТМС у пациентов с актуальной психотической симптоматикой, а при сохранении тенденции к ухудшению состояния, решения вопроса о досрочном прекращении курса стимуляции. Зарегистрированное ятрогенное гипоманиакальное состояние (2,2%), в отличие от субпсихотического, не требовало дополнительных мер и разрешилось самостоятельно.
- Терапевтическая эффективность рТМС определяется рядом биологических параметров. Установлено, что анализ особенностей исходной фоновой ЭЭГ и вызванных потенциалов, определение воспалительных и аутоиммунных маркеров, а также исследование особенностей нейрокогнитивного функционирования имеют высокое прогностическое значение.
4.1. Нейрофизиологическое исследование позволило выявить несколько показателей (по данным ЭЭГ), ассоциированных с благоприятной терапевтической траекторией, к которым относились большая когерентность в бета1-поддиапазоне и меньшая исходная спектральная мощность волн тета-диапазона.
4.2. Нейроиммунологическое исследование перед проведением рТМС позволило выявить прогностически значимые различия иммунологических показателей у пациентов с резистентной шизофренией, которые могут использоваться для прогноза терапевтического ответа на рТМС. Установлено, что для благоприятной терапевтической траектории характерно исходное незначительное повышение активности ЛЭ и α1-ПИ, при этом у 75,0% пациентов после курса рТМС отмечалась относительная нормализация иммунологических показателей, что является объективным маркером снижения интенсивности патологического процесса в мозге; нейтральная терапевтическая траектория характеризовалась изначально выраженным повышением активности ЛЭ и α1-ПИ и в 77,8% ухудшением иммунологических показателей на фоне проведения рТМС; для отрицательной терапевтической траектории исходно характерна низкая активность ЛЭ в сочетании с аутоиммунным компонентом, при этом на фоне рТМС с одинаковой частотой (50,0%) встречаются случаи, как с положительной, так и с отрицательной динамикой иммунологических показателей.
4.3. Нейропсихологическое исследование выявило, что для благоприятной терапевтической траектории был характерен комплекс нарушений избирательности психических процессов, связанный с дисфункцией правого полушария; для нейтральной терапевтической траектории были характерны нарушения регуляции произвольной деятельности, обработки слухоречевой информации, а также нарушения пространственного анализа и синтеза, выраженные в разной степени; для отрицательной терапевтической траектории характерен комплекс выраженных нарушений произвольной регуляции мыслительных процессов, связанный с дисфункцией префронтальной коры левого полушария.
Практические рекомендации и
перспективы дальнейшей разработки темы
Проводя анализ полученных результатов, можно выделить ряд характерных особенностей применения рТМС в отношении резистентных состояний при шизофрении:
- Выраженность терапевтического эффекта рТМС обладает межиндивидуальной вариабельностью, что в данном исследовании было продемонстрировано различными темпами редукции симптоматики при рассмотрении психометрических данных.
- Безопасность проведения рТМС напрямую зависит от клинико-психопатологических особенностей состояния. С учетом потенциального риска обострения психотической симптоматики более безопасно использовать рТМС для лечения инертных хронических состояний с резистентной симптоматикой, исключая периоды обострения. Наличие в статусе актуальной бредовой симптоматики требует пребывания пациента в стационаре для реализации противорезистентных мероприятий.
- Метод рТМС, предполагая под собой селективность воздействия, проявляет тропность к определенным клинико-психопатологическим образованиям, в меньшей степени оказывая влияние на общую картину заболевания. Ввиду этого, для более точного ранжирования эффекта от лечения, необходимо, наряду с психометрическими шкалами, предполагающими комплексную оценку состояния, использовать шкалы для оценки целевого кластера симптомов.
- Рассмотрение особенностей терапевтического патокинеза различных разновидностей резистентных состояний свидетельствует о возможности изменения терапевтической тактики для улучшения конечных результатов. В соответствии с гипотезой о реализации терапевтических эффектов рТМС посредством активизации механизмов нейропластичности, оправдано и допустимо варьировать продолжительность курса, соблюдая при этом основные принципы безопасности. В данном исследовании было показано, что в ряде случаев завершение курса лечения не соответствовало максимальному результату или его стабилизации.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
Публикации в рецензируемых журналах, рекомендованных ВАК
- Помыткин, А. Н. Эффективность высокочастотной ритмической транскраниальной магнитной стимуляции при эндогенных депрессивных расстройствах в юношеском возрасте / А. Н. Помыткин, В. Г. Каледа,
И. В. Клочкова, И. С. Лебедева // Журнал неврологии и психиатрии им.
C. Корсакова. – 2019. – Т. 119. – №. 12. – С. 38-45. - Pomytkin, A. N. Efficacy of High-Frequency Rhythmic Transcranial Magnetic Stimulation in Endogenous Depressive Disorders at Juvenile Age
/ A. N. Pomytkin, V. G. Kaleda, I. V. Klochkova, I. S. Lebedeva // Neuroscience and Behavioral Physiology. – 2020. – Т. 50. – №. – С. 972-979. - Помыткин, А. Н. Ритмическая транскраниальная магнитная стимуляция в терапии резистентных депрессий при шизофрении
/ А. Н. Помыткин, И. С. Лебедева, Д. В. Тихонов В. Г. Каледа // Журнал неврологии и психиатрии им. C.C. Корсакова. – 2021. – Т. 121. – №. 5-2. – С. 99-105. - Помыткин, А. Н. Эффективность ритмической транскраниальной магнитной стимуляции дорсолатеральной префронтальной коры при терапии эндогенных депрессивных расстройств (клинические и нейрофизиологические аспекты) / А. Н. Помыткин, Я. Р. Паникратова, И. С. Лебедева // Психиатрия. – 2016. – №. 3. – С. 68-69a.
- Помыткин, А. Н. Современные аспекты терапевтической резистентности при шизофрении / Д. В. Тихонов, А. Н. Помыткин, В. Г. Каледа // Психическое здоровье. – 2021. – №. 12. – С. 79-89.
- Помыткин, А. Н. Ритмическая транскраниальная магнитная стимуляция в терапии резистентной шизофрении / А. Н. Помыткин // Психиатрия. – 2022. – Т. 20, № S3(2). – С. 32-33.
- Помыткин, А. Н. Аугментация терапии резистентной шизофрении методом ритмической транскраниальной магнитной стимуляции. / А. Н. Помыткин, Д. В. Тихонов, В. Г. Каледа // Журнал неврологии и психиатрии им. С.С. Корсакова. 2023;123(8):107‑114.
Тезисы, представленные в материалах научных конференций и конгрессов
- Помыткин, А. Н. Эффективность рТМС левой дорсолатеральной префронтальной коры при терапии эндогенных депрессивных расстройств (клинические и нейрофизиологические данные) / А. Н. Помыткин,
Я. Р. Паникратова // Школа молодых ученых "Шизофрения: настоящее, взгляд в будущее" : Материалы III-ей Всероссийской Костромской школы молодых ученых и специалистов в области психического здоровья, Москва-Кострома, 19–22 апреля 2016 года / ФГБНУ НЦПЗ. – Москва-Кострома: Научный центр психического здоровья, 2016. – С. 272-276. - Помыткин, А. Н. Использование ритмической ТМС в комплексной терапии резистентных расстройств при параноидной шизофрении / А. Н. Помыткин // Психиатрическая наука в истории и перспективе : Материалы Юбилейной Всероссийской научно-практической конференции с международным участием, посвященной 75-летию Научного центра психического здоровья, Москва, 07 июня 2019 года. – Москва: ФГБНУ НЦПЗ, 2019. – С. 318-323.
- Pomytkin, A. N. High-frequency rTMS in the treatment of depressive symptoms in schizophrenia: a neurophysiological profile of respondents and nonresponders / A. N. Pomytkin, V. G. Kaleda, I. S. Lebedeva // European Psychiatry. – 2022. – Т. 65. – №. S1. – С. S774-S774.
[1] Совместно с руководителем лабораторией нейровизуализации и мультимодального анализа, д.б.н. И.С. Лебедевой
[2] Совместно с ведущим научным сотрудником отдела юношеской психиатрии, к.п.н.
И.В. Плужниковым
[3] Совместно с ведущим научным сотрудником лаборатории нейроиммунологии, к.б.н. С.А. Зозулей

